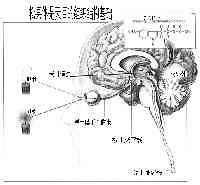
松果体(天目)分泌的美乐托宁对健康的影响
-------- 《转法轮》
现代科学家将松果体直接叫做“第三只眼”(1)。人们直到1950年发现了松果体激素-美乐托宁后才对其功能有所了解。最近,我们发现在大法弟子唾液中美乐托宁的水平增高。我们这一发现和当今科学新进展有助于解释法轮大法修炼中的一些现象。例如为什么修炼者能保持身体健康,为什么他们会有在炼功时能看见另外空间景象这一类的特殊功能。这篇小综述总结了近年来有关人体美乐托宁和松果体的知识和其临床应用。
松果体是一个神秘的器官, 三百年前法国哲学家雷诺.底卡地斯将之描述为“灵魂的座椅”。现在已经很清楚地知道松果体调解所有的内分泌器官的功能而被称为“内分泌器官总司令”。《转法轮》一书中指出,松果体是天目的基础(图1),松果体在维持健康中,对环境压力产生适应性反应, 这是通过人体,生命和宇宙的相互作用实现的。因此,松果体被认为是至关重要的器官(2)。
美乐托宁的合成是通过光节律在转译水平上调解的。合成出的美乐托宁可调解情绪,睡眠,性行为,繁殖,免疫系统和生理节奏(3)。美乐托宁是通过高亲和力的受体完成这些调节功能的。这些受体属于与G蛋白相联系的,具有七次穿膜结构的受体,存在于眼,肾,胃肠道。血管和脑(4)。另有证据表明美乐托宁在衰老及与衰老相关的疾病中的作用。这可能与其有效地消除自由基(或抗氧化)能力有关(5,6)。美乐托宁作为抗氧化剂的潜在临床意义是巨大的。它可能对治疗许多病理生理疾病状态有效。能用它治疗的包括各种癌症,高血压,肺部疾患和诸如老年性痴呆的各种神经退行性病变(3,7-9)。此外,有报道美乐托宁对免疫系统缺陷小鼠有免疫调节功能,提示我们它可能改善免疫状况(11-12)。
众所周知,修炼法轮大法能使人保持健康并能使诸如神经紧张,癌症,白血病,自身免疫病,失眠这一类的疾病痊愈。此外,炼法轮功也能逆转衰老过程。可以推测,由松果体分泌的美乐托宁水平变化可能是对法轮功调节健康的原理之一。
衰老,失眠,和乳腺癌是绝经期妇女的主要疾病。美乐托宁可能与绝经期相关过程如乳腺癌和衰老有关。尽管美乐托宁替代疗法治疗所有绝经期妇女仍未能通过,但有证据表明美乐托宁确能改善更年期妇女综合症 (13)。在绝经期妇女开始炼法轮功后恢复月经是司空见惯的。可以进一步推测,内源性美乐托宁的增加有可能导致绝经期妇女练功后恢复了月经。
随着人的衰老,夜间血清中美乐托宁浓度及其生理效应降低。有些研究人员提出美乐托宁对衰老相关疾病有作用(14,15)。虽然尚无证据表明美乐托宁在人体的抗衰老效应,在小鼠和大鼠身上做的实验表明松果体可能是掌管衰老的内源性时钟(16-17)。有临床证据表明美乐托宁在诸如生物时钟节奏,睡眠,情绪也许还包括繁殖,肿瘤生长和衰老方面有生物调节作用(3)。尽管如此,有些科学家表示,美乐托宁对人体生理和病理生理的作用仍待近一步确定(18)。
综上所述,很有必要对在法轮大法修炼者身上观察到的与健康相关的现象及美乐托宁在其中所起的作用进行深入的研究。
参考文献:
1. Booth, F. M. 1987. The human pineal gland: a review of the "third eye" and the effect of light. Aust N Z J Ophthalmol 15:329.
2. Pettersson, P. 2000. The pineal gland - The bridge between the physical and spiritual reality. http://www.alphaomega.se/english/pineal.html.
3. Brzezinski, A. 1997. Melatonin in humans. N Engl J Med 336:186.
4. Reppert, S. M. 1997. Melatonin receptors: molecular biology of a new family of G protein-coupled receptors. J Biol Rhythms 12:528.
5. Beyer, C. E., J. D. Steketee, and D. Saphier. 1998. Antioxidant properties of melatonin--an emerging mystery [published erratum appears in Biochem Pharmacol 1999 May 1;57(9):1077]. Biochem Pharmacol 56:1265.
6. Lahiri, D. K., and C. Ghosh. 1999. Interactions between melatonin, reactive oxygen species, and nitric oxide. Ann N Y Acad Sci 893:325.
7. Wetterberg, L. 1999. Melatonin and clinical application. Reprod Nutr Dev 39:367.
8. Reiter, R. J., J. Cabrera, R. M. Sainz, J. C. Mayo, L. C. Manchester, and D. X. Tan. 1999. Melatonin as a pharmacological agent against neuronal loss in experimental models of Huntington"s disease, Alzheimer"s disease and parkinsonism. Ann N Y Acad Sci 890:471.
9. Pappolla, M. A., Y. J. Chyan, B. Poeggeler, P. Bozner, J. Ghiso, S. P. LeDoux, and G. L. Wilson. 1999. Alzheimer beta protein mediated oxidative damage of mitochondrial DNA: prevention by melatonin. J Pineal Res 27:226.
10. Maestroni, G. J., A. Conti, and W. Pierpaoli. 1988. Pineal melatonin, its fundamental immunoregulatory role in aging and cancer. Ann N Y Acad Sci 521:140.
11. Caroleo, M. C., D. Frasca, C. Mancini, G. Nistico, and G. Doria. 1990. Effect of melatonin on T helper cell activity. Pharmacol Res 22 Suppl 3:53.
12. Caroleo, M. C., D. Frasca, G. Nistico, and G. Doria. 1992. Melatonin as immunomodulator in immunodeficient mice. Immunopharmacology 23:81.
13. FLG, P. o. Experience-sharing articles. http://www.minghui.org/eng.html.
14. van Coevorden, A., J. Mockel, E. Laurent, M. Kerkhofs, M. L~Hermite-Baleriaux, C. Decoster, P. Neve, and E. Van Cauter. 1991. Neuroendocrine rhythms and sleep in aging men. Am J Physiol 260:E651.
15. Reiter, R. J. 1995. The pineal gland and melatonin in relation to aging: a summary of the theories and of the data. Exp Gerontol 30:199.
16. Dilman, V. M., V. N. Anisimov, M. N. Ostroumova, V. K. Khavinson, and V. G. Morozov. 1979. Increase in lifespan of rats following polypeptide pineal extract treatment. Exp Pathol (Jena) 17:539.
17. Pierpaoli, W., and W. Regelson. 1994. Pineal control of aging: effect of melatonin and pineal grafting on aging mice. Proc Natl Acad Sci U S A 91:787.
18. Reppert, S. M., and D. R. Weaver. 1995. Melatonin madness. Cell 83:1059.